
علل و درمان های درد دندان های مجاور بعد از کاشت ایمپلنت های دندانی
0 نظرها
/
چه چیزی می تواند باعث ایجاد ناراحتی در دندان های کنار ایمپلنت های دندانی شما شود؟ انتظار دندانی قابل درک است، اما تجربه درد یا حساسیت در دندان های مجاور بسیار شایع است.آیا بعد از کاشت ایمپلنت های دندان احساس ناراحتی می کنید؟ نیازی به نگرانی نیست. در واقع احساس درد، فشار یا حساسیت خفیف به دنبال این فرایند درمان بسیار شایع است و احتمالاً نشانه ای از بهبودی بدن شما است.

آیا افراد بزرگسال می توانند سیلانت دندانی استفاده کنند؟
سیلانت های دندانی به عنوان رزین مایع شروع می شوند. این مایع که روی سطوح جونده دندان نقاشی می شود، هر گونه شیار و حفره کوچکی را پر می کند.سیلانت های دندانی یک راه ایمن و مؤثر برای جلوگیری از پوسیدگی برای کودکان هستند. اما آیا آنها فقط برای کودکان هستند؟ از این گذشته، پوسیدگی دندان هنوز در هر سنی ممکن است اتفاق بیفتد. چرا افراد بزرگسال نیز نباید از سیلانت دندان استفاده کنند؟

چرا بعد از مسواک زدن برای خوردن باید 30 دقیقه صبر کرد؟
بسیاری از دندانپزشکان توصیه می کنند 30 دقیقه بعد از مسواک زدن قبل از نوشیدن هر چیزی صبر کنید. اما چرا این دوره انتظار ضروری است؟ وقتی خیلی زود بعد از مسواک زدن آب می خورید چه اتفاقی می افتد؟ در این مقاله، دلایل این توصیه رایج دندانپزشکی را با عمق بیشتری بررسی خواهیم کرد و خطرات بالقوه عدم رعایت آن را توضیح خواهیم داد.
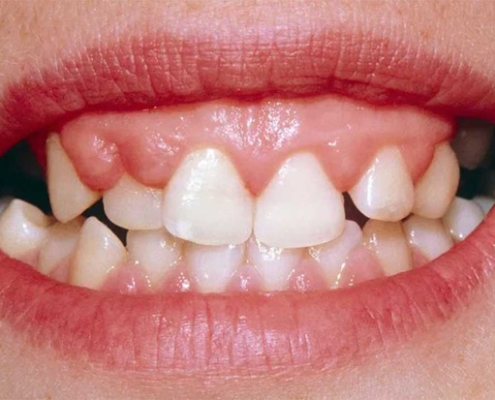
چرا لثه های من روی دندان هایم همپوشانی دارند؟
رشد بیش از حد لثه که در اصطلاح پزشکی به رشد بیش از حد لثه یا هیپرپلازی لثه نیز گفته می شود، وضعیتی است که در آن بافت لثه (جینجیوا) اطراف دندان ها بزرگ و متورم می شود یا بیش از حد رشد می کند. این می تواند منجر به افزایش حجم لثه ها به بیرون و شروع به همپوشانی یا پوشاندن کامل دندان ها شود.

چه چیزی دندان ها را در جای خود نگه می دارد؟
آیا تا به حال به این فکر کرده اید که چه چیزی دندان های شما را در جای خود نگه می دارد؟ پاسخ آنقدرها هم که فکر می کنید ساده نیست. دندان های شما توسط ترکیبی از عوامل، از جمله رباط پریودنتال، سمان و استخوان آلوئولار نگه داشته می شوند.درک اینکه چه چیزی دندان های شما را در جای خود نگه می دارد برای حفظ سلامت دهان و دندان مهم است. با مراقبت از دندان ها و لثه ها، می توانید اطمینان حاصل کنید که آنها برای سال های آینده محکم در جای خود باقی می مانند.
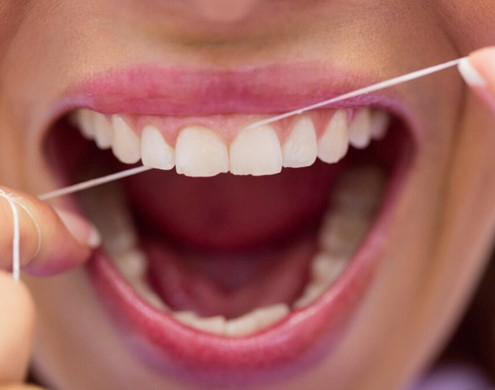
آیا نزدیک شدن به لثه هنگام نخ دندان کشیدن خوب است یا بد؟
وقتی صحبت از نخ دندان می شود، ممکن است به این موضوع فکر کنید که آیا نزدیک شدن به لثه ها خوب است یا بد. برخی افراد از نزدیک شدن به لثه های خود با نخ دندان اجتناب می کنند، در حالی که برخی دیگر معتقدند که برای بهداشت مناسب دهان و دندان این کار لازم است. بنابراین، آیا هنگام استفاده از نخ دندان باید لثه های خود را لمس کرد؟ پاسخ مثبت است، اما با احتیاط.
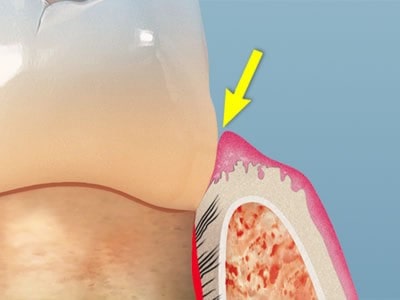
شیار لثه یا ژینژیوال سالکوس چیست؟
ژینژیوال سالکوس (یا شیار لثه) آن برآمدگی کوچک در دهان شما است که در آن دندان ها به لثه های شما می رسند. تمیز نگه داشتن آن برای سلامت لثه و دندان بسیار مهم است. بهداشت خوب دهان و دندان مهم است - و هرچه بیشتر در مورد دهان خود بدانید، بهتر می توانید در طول زندگی خود از آن مراقبت کنید.

آیا استرس و اضطراب می تواند باعث درد لثه شود؟
یکی از ارتباطاتی که تحقیقات در حال بررسی آن هستند، اثرات استرس و اضطراب طولانی مدت بر سلامت لثه است. آیا افزایش هورمون های استرس و اضطراب مزمن می تواند روی مشکلات لثه مانند تورم، حساسیت و خونریزی تأثیر منفی داشته باشد؟ بیایید مکانیسم های احتمالی زیربنای این ارتباط را تجزیه و تحلیل کنیم.

چرا دندانپزشک روی دندان های برخی بیماران فلوراید می زند؟
فلوراید نقش مهمی در مدیریت پوسیدگی مبتنی بر شواهد در طول عمر ایفا می کند. فلوراید موضعی به تقویت مینای دندان در برابر حملات اسیدی کمک می کند و باعث افزایش معدنی سازی مجدد می شود. همچنین باکتری های موجود در بیوفیلم را مهار می کند که فرآیند پوسیدگی را آغاز می کنند. بهینه سازی قرار گرفتن در معرض فلوراید یک ستون سلامت پیشگیرانه دهان و دندان است.

درمان ارتودنسی با الاینرهای شفاف در بیماران مبتلا به پریودنتیت
ارتباط شدیدی بین فشردگی و پریودنتیت وجود دارد، زیرا جابجایی دندان های قدامی در اثر بیماری پریودنتال افزایش می یابد که منجر به فشردگی بیشتر در قوس دندانی پایین می شود، که در نتیجه سلامت پریودنتال را مختل می کند.برای درمان بیماران مبتلا به مال اکلوژن ثانویه یا در افرادی که تشدید مال اکلوژن موجود مرتبط با بیماری پریودنتال وجود دارد، ارتودنسی ترکیب با درمان پریودنتال و پروتز مورد نیاز است.
